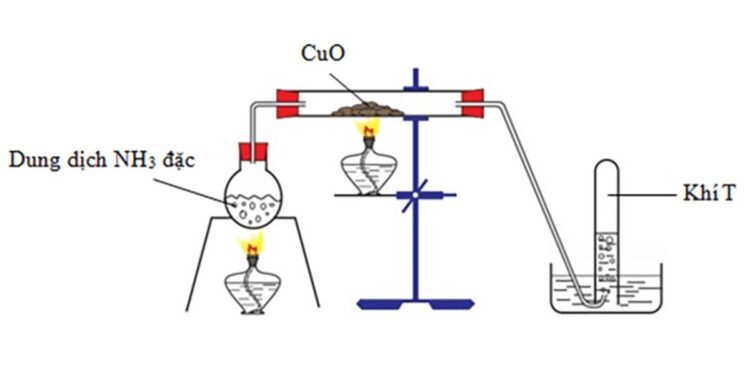
Phản ứng giữa NH₃ (amoniac) và CuO (đồng(II) oxit) là một minh chứng sinh động cho sự kỳ diệu của hóa học, nơi các chất tưởng chừng quen thuộc lại mang đến những biến đổi thú vị. Phản ứng này không chỉ đóng vai trò quan trọng trong phòng thí nghiệm mà còn ứng dụng rộng rãi trong công nghiệp, từ xử lý khí thải đến tái chế kim loại. Cùng Hóa Học Phổ Thông Khám phá cơ chế và ý nghĩa của phản ứng NH3 + CuO sẽ giúp bạn hiểu sâu hơn về sức mạnh của hóa học và tiềm năng ứng dụng vô tận của nó.
TÓM TẮT
Cơ chế phản ứng NH3 + CuO
Phản ứng giữa amoniac (NH₃) và đồng(II) oxit (CuO) là một ví dụ sinh động về quá trình oxy hóa – khử, nơi các chất đơn giản lại tạo nên những biến đổi đầy bất ngờ. Khi đun nóng, tính chất hóa học của nh3 tương tác với CuO để giải phóng kim loại đồng (Cu), nước (H₂O), và khí nitơ (N₂). Đây không chỉ là một phản ứng hóa học phổ biến trong phòng thí nghiệm mà còn có ý nghĩa lớn trong công nghiệp xử lý và tái chế kim loại.
2NH₃ + 3CuO → 3Cu + N₂ + 3H₂O
Phương trình này cho thấy NH₃ đóng vai trò là chất khử, trong khi CuO là chất oxy hóa. Sản phẩm chính của phản ứng là đồng kim loại, khí nitơ và nước – những hợp chất có ứng dụng rộng rãi trong đời sống và sản xuất.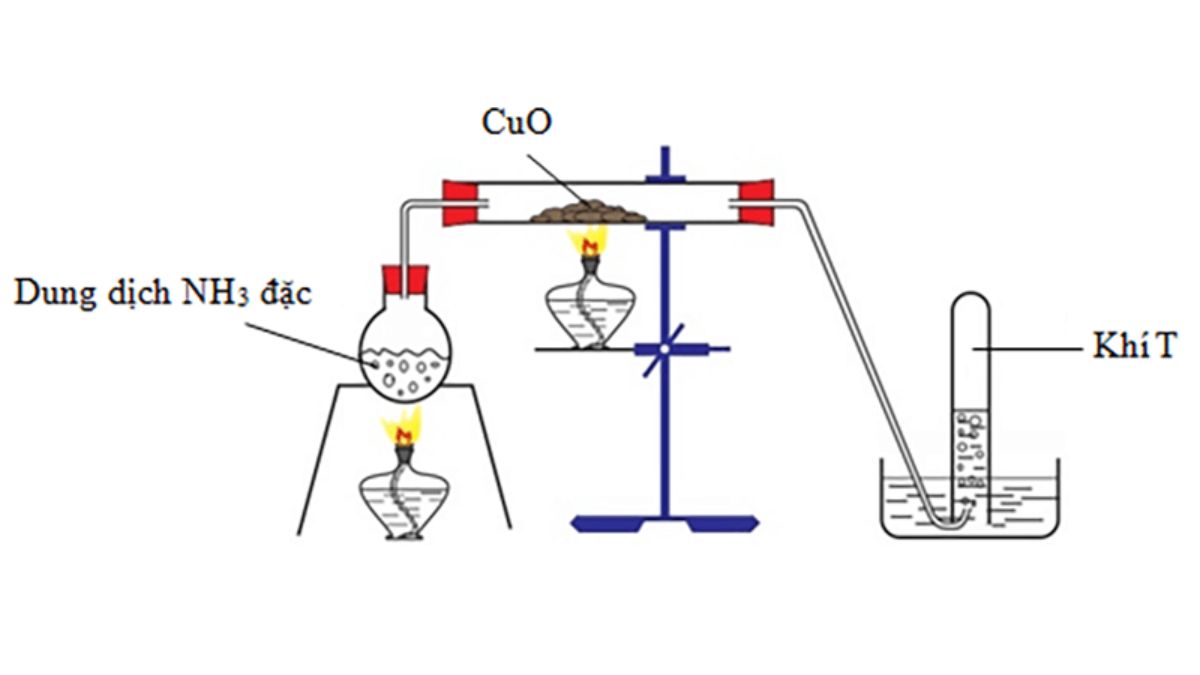
Vai trò của NH₃ trong phản ứng
NH₃ là một hợp chất giàu năng lượng, có khả năng nhường
electron trong quá trình phản ứng. Khi được đun nóng, NH₃ bị phân hủy và tham gia phản ứng với CuO, tạo ra khí nitơ và nước.
2NH₃ → N₂ + 6H⁺ + 6e⁻
Như vậy, NH₃ đã trải qua quá trình oxy hóa, mất electron và giải phóng khí nitơ (N₂), một loại khí trơ phổ biến trong khí quyển.
Vai trò của CuO trong phản ứng
CuO là một hợp chất oxit của kim loại đồng, có khả năng nhận electron trong quá trình phản ứng. Dưới tác dụng của nhiệt, CuO bị khử thành đồng kim loại:
Cu²⁺ + 2e⁻ → Cu
Đây là một quá trình khử, trong đó ion Cu²⁺ nhận electron và chuyển thành đồng kim loại (Cu), xuất hiện dưới dạng các mảnh hoặc lớp rắn màu đỏ nâu.
Điều kiện xảy ra phản ứng NH3 + CuO
Nhiệt độ: Phản ứng này chỉ diễn ra khi được đun nóng đủ mạnh, do cần năng lượng để kích hoạt sự phân hủy của NH₃ và thúc đẩy CuO nhận electron.
Tỉ lệ mol: Để phản ứng xảy ra hoàn toàn, cần đảm bảo đúng tỷ lệ 2:3 giữa NH₃ và CuO. Nếu tỉ lệ không chính xác, có thể tạo ra sản phẩm phụ hoặc dư thừa một trong các chất tham gia.
Môi trường: Phản ứng được thực hiện trong không gian kín hoặc môi trường ít oxy, nhằm tránh oxy ngoài không khí ảnh hưởng đến quá trình khử CuO.
Khám phá ngay chuyên mục “Tài liệu hóa học phổ thông” để nắm vững kiến thức từ cơ bản đến nâng cao!
Hiện tượng quan sát được khi phản ứng xảy ra
Ban đầu, CuO có màu đen. Khi phản ứng diễn ra, CuO bị khử thành đồng kim loại, tạo ra lớp màu đỏ hoặc nâu đỏ bám trên bề mặt. Khí nitơ (N₂) thoát ra trong quá trình phản ứng, không màu và không mùi. Nước được tạo ra dưới dạng hơi, có thể nhìn thấy khi ngưng tụ trên thành bình thí nghiệm.
Phản ứng giữa NH3 + CuO là một phản ứng tỏa nhiệt, giải phóng năng lượng dưới dạng nhiệt. Nhiệt lượng này có thể làm tăng nhiệt độ của hệ thống, giúp phản ứng diễn ra nhanh hơn. Đây là lý do phản ứng này thường được dùng để minh họa cho các quá trình tỏa nhiệt trong hóa học.
Ứng dụng của phản ứng NH3 + CuO
Tái chế kim loại đồng: Quá trình này giúp thu hồi đồng từ các hợp chất oxit, góp phần vào việc tái chế và tiết kiệm tài nguyên.
Xử lý khí thải: NH₃ thường được sử dụng trong các hệ thống khử oxit nitơ (NOx) từ khí thải công nghiệp. Tuy phản ứng NH3 + CuO không trực tiếp loại bỏ NOx, nhưng nó minh họa rõ cơ chế khử bằng amoniac.
Thí nghiệm giáo dục: Phản ứng này là một ví dụ điển hình về phản ứng oxy hóa – khử, thường được dùng trong các bài thực hành hóa học để giúp học sinh hiểu rõ cơ chế electron trong phản ứng.
Phản ứng này không chỉ có giá trị học thuật mà còn có ứng dụng thực tiễn rõ rệt trong nhiều lĩnh vực. Nó minh chứng cho vai trò của hóa học trong việc tái chế tài nguyên, bảo vệ môi trường, và đào tạo thế hệ trẻ về khoa học.
Phản ứng NH3 + CuO là một ví dụ đầy ý nghĩa về sự kết hợp giữa lý thuyết và ứng dụng. Hiểu rõ cơ chế này không chỉ giúp nắm bắt bản chất của các phản ứng hóa học mà còn mở ra nhiều cơ hội áp dụng trong thực tiễn đời sống và công nghiệp.
Kết luận
Phản ứng NH3 + CuO không chỉ là một hiện tượng hóa học đơn thuần mà còn mở ra những giải pháp thực tiễn cho nhiều lĩnh vực như bảo vệ môi trường và tái chế tài nguyên. Sự kết hợp giữa kiến thức khoa học và ứng dụng thực tế đã chứng minh rằng hóa học không chỉ giới hạn trong lý thuyết mà còn gắn liền với cuộc sống. Tiếp tục tìm hiểu thêm những phản ứng thú vị khác sẽ là bước đệm để bạn khám phá sâu hơn về thế giới hóa học đầy màu sắc này.
Có thể bạn quan tâm: