Hidro, một nguyên tố đơn giản nhưng có vai trò cực kỳ quan trọng trong nhiều phản ứng hóa học và ứng dụng trong cuộc sống. Với đặc điểm hóa học độc đáo, Hidro không chỉ góp mặt trong nhiều phản ứng hóa học mà còn được ứng dụng rộng rãi trong nhiều ngành công nghiệp. Bài viết này hoahocphothong sẽ cung cấp một cái nhìn tổng quan, chi tiết và toàn diện về tính chất hóa học của Hidro cũng như các ứng dụng thực tiễn của nó trong nghiên cứu và sản xuất.
TÓM TẮT
Khái quát về Hidro
Hidro (ký hiệu hóa học H) là nguyên tố nhẹ nhất trong bảng tuần hoàn với số hiệu nguyên tử là 1 và nguyên tử khối là 1. Cấu trúc của Hidro khá đơn giản với một proton và một electron duy nhất. Phân tử Hidro tồn tại chủ yếu dưới dạng H2, một phân tử khí không màu, không mùi, không vị, dễ cháy và rất phổ biến trong tự nhiên. Hidro là nguyên tố có tính khử mạnh và thường tham gia vào các phản ứng tạo ra năng lượng hoặc các hợp chất mới.
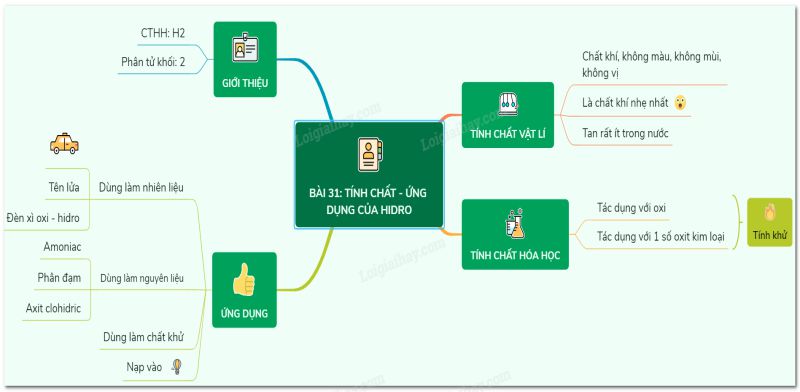
Về cấu hình electron, Hidro nằm trong chu kỳ 1, nhóm IA của bảng tuần hoàn. Nó có khả năng kết hợp với nhiều nguyên tố khác, đặc biệt là oxi và các kim loại, để tạo ra những hợp chất hữu ích. Đặc biệt, Hidro có khả năng tỏa nhiệt khi tham gia các phản ứng hóa học, nhất là khi phản ứng với oxi. Khám phá thêm về tính chất hóa học của hidro cùng mình nhé!
Tính chất hóa học của Hidro
Tính chất hóa học của phi kim của Hidro: nguyên tố có khả năng tham gia vào nhiều loại phản ứng hóa học khác nhau. Tính chất hóa học của Hidro được thể hiện qua những phản ứng quan trọng sau:
Hidro phản ứng với oxi
Hidro phản ứng mạnh mẽ với oxi để tạo thành nước (H2O). Đây là một phản ứng tỏa nhiệt, và trong điều kiện thích hợp, hỗn hợp của Hidro và oxi có thể gây nổ. Phản ứng này là một trong những tính chất hóa học nổi bật nhất của Hidro, được ứng dụng rộng rãi trong các ngành công nghiệp.
Phương trình phản ứng:
2H2 + O2 → 2H2O
Khi Hidro và oxi kết hợp với nhau theo tỷ lệ thể tích 2:1, hỗn hợp sẽ trở nên cực kỳ dễ nổ. Đây là một trong những cơ sở để chế tạo động cơ tên lửa và các thiết bị tạo năng lượng mạnh.
Hidro phản ứng với oxit kim loại
Hidro là một chất khử mạnh, có khả năng khử nhiều oxit kim loại để tạo thành kim loại tự do và nước. Phản ứng này thường xảy ra ở nhiệt độ cao và được ứng dụng nhiều trong công nghệ luyện kim.
Ví dụ phản ứng:
FeO + H2 → Fe + H2O
CuO + H2 → Cu + H2O
Trong thực tế, phản ứng giữa Hidro và đồng oxit (CuO) xảy ra mạnh mẽ ở khoảng 400 độ C, tạo ra đồng nguyên chất và hơi nước. Đây là phản ứng rất quan trọng trong việc điều chế kim loại từ các oxit của chúng.
Hidro phản ứng với phi kim
Hidro có thể phản ứng với nhiều phi kim khác nhau để tạo ra các hợp chất hóa học mới. Ở nhiệt độ cao, Hidro có khả năng kết hợp với các phi kim như lưu huỳnh (S) hoặc phốtpho (P) để tạo thành hydrua.
Phương trình phản ứng:
H2 + S → H2S (khí hydro sunfua)
2H2 + O2 → 2H2O (nước)
Phản ứng giữa Hidro và lưu huỳnh tạo ra khí hydro sunfua (H2S), một chất khí có mùi trứng thối đặc trưng và độc hại.
Hidro phản ứng với halogen
Hidro có thể phản ứng với các phi kim halogen như flo (F2), clo (Cl2), brom (Br2), và iốt (I2) để tạo ra khí hidro halogenua, một hợp chất dễ tan trong nước, tạo thành dung dịch axit.
Phương trình phản ứng:
H2 + F2 → 2HF (axit flohiđric)
H2 + I2 → 2HI (axit iođhiđric)
Axit flohiđric (HF) là một chất quan trọng trong nhiều ngành công nghiệp, đặc biệt là trong chế tạo và làm sạch thủy tinh.
Hidro phản ứng với kim loại
Hidro có thể phản ứng với nhiều kim loại ở nhiệt độ cao để tạo ra các hợp chất hidrua kim loại (MHx). Đây là phản ứng giúp tạo ra các loại muối hidrua, có vai trò quan trọng trong nghiên cứu và sản xuất.
Ví dụ phản ứng:
Mg + H2 → MgH2 (magie hidrua)
Na + H2 → NaH (natri hidrua)
Những muối này được ứng dụng trong các lĩnh vực như tích trữ năng lượng và tạo nhiên liệu sạch.
Ứng dụng của Hidro trong công nghiệp
Với những tính chất hóa học phong phú, Hidro được ứng dụng rộng rãi trong nhiều lĩnh vực của đời sống, từ giao thông vận tải, luyện kim, cho đến y tế.
Khám phá ngay chuyên mục “Tài liệu hóa học phổ thông” để nắm vững kiến thức từ cơ bản đến nâng cao!
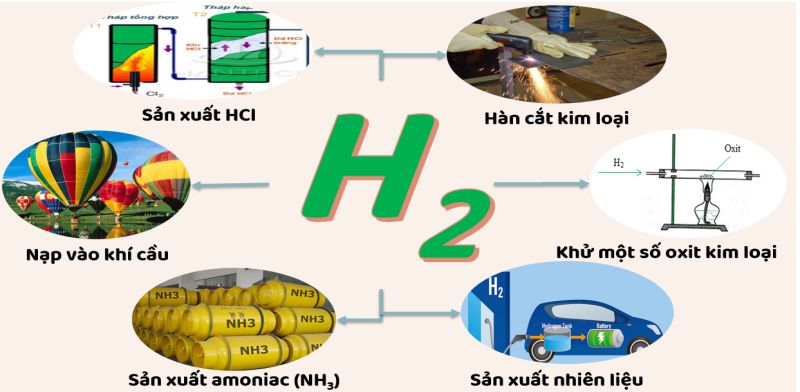
Sử dụng Hidro trong giao thông vận tải
Hidro được sử dụng làm nhiên liệu cho động cơ tên lửa nhờ khả năng sinh nhiệt mạnh mẽ trong các phản ứng cháy. Bên cạnh đó, Hidro cũng được dùng để bơm khinh khí cầu, giúp các phương tiện này bay lên cao và duy trì độ cao trong không khí.
Hidro trong ngành hóa chất
Hidro là nguyên liệu chính để sản xuất các hợp chất hữu ích trong công nghiệp như amoniac (NH3) dùng trong phân bón, hoặc axit clohidric (HCl). Đây là hai sản phẩm quan trọng trong nông nghiệp và nhiều lĩnh vực khác của sản xuất công nghiệp.
Sử dụng trong luyện kim
Hidro được sử dụng để khử oxit kim loại, điều chế các kim loại nguyên chất như sắt, đồng, kẽm, v.v. Ngoài ra, Hidro còn được sử dụng trong đèn xì oxi-hidro để hàn cắt kim loại, giúp tạo ra các mối hàn bền chắc.
Ứng dụng trong chăm sóc sức khỏe
Trong lĩnh vực y tế, Hidro được ứng dụng trong các sản phẩm chống oxy hóa, giúp ngăn ngừa quá trình lão hóa trong cơ thể con người. Quá trình điện phân Hidro giúp tạo ra nước giàu ion H2, được cho là có khả năng cải thiện sức khỏe và phòng ngừa bệnh tật.
Kết luận
Hidro là một nguyên tố không thể thiếu trong hóa học và nhiều ngành công nghiệp. Với khả năng kết hợp với nhiều nguyên tố khác và tham gia vào các phản ứng quan trọng, Hidro đóng vai trò quan trọng trong nhiều lĩnh vực từ sản xuất, giao thông vận tải, đến chăm sóc sức khỏe. Hiểu rõ tính chất hóa học của Hidro sẽ giúp chúng ta khai thác tối đa các tiềm năng của nguyên tố này trong nghiên cứu và ứng dụng thực tiễn.
Có thể bạn quan tâm:









