Trong hóa học phổ thông, một trong những nguyên tố thường gặp nhưng không phải lúc nào cũng được khám phá đầy đủ là lưu huỳnh – hay còn được gọi tắt là so. Vậy so là nguyên tố gì? Nó có vai trò thế nào trong tự nhiên, đời sống và các phản ứng hóa học? Bài viết này sẽ giúp bạn khai thác toàn diện về lưu huỳnh: từ đặc điểm nguyên tử, cấu hình điện tử cho đến ứng dụng thực tiễn, tất cả đều được trình bày một cách dễ hiểu và sinh động cho học sinh, giáo viên và người yêu thích hóa học.
Để hiểu rõ hơn về cách phân loại nguyên tố như so, bạn có thể tham khảo nội dung liên quan về nguyên tố mg là nguyên tố gì, rất hữu ích để so sánh tính chất hóa học giữa các nguyên tố phi kim và kim loại nhẹ.
TÓM TẮT
- 1 Tổng quan: So là nguyên tố gì trong bảng tuần hoàn?
- 2 Lưu huỳnh có ở đâu trong tự nhiên?
- 3 Tính chất hóa học đặc trưng của lưu huỳnh
- 4 Các hợp chất quan trọng của so (S)
- 5 Lưu huỳnh – nguyên tố không thể thiếu trong đời sống
- 6 Hỏi – Đáp Nhanh: Những câu hỏi phổ biến về “so là nguyên tố gì”
- 7 Bổ sung kiến thức: Liên hệ với các nguyên tố phi kim khác
- 8 Hình ảnh minh họa
- 9 Kết luận
Tổng quan: So là nguyên tố gì trong bảng tuần hoàn?
Lưu huỳnh (ký hiệu là S, đọc là “so” theo cách viết âm Hán – Việt) là nguyên tố hóa học thuộc nhóm VIA (nhóm Oxi), chu kỳ 3 trong bảng tuần hoàn. Đây là một phi kim điển hình với số hiệu nguyên tử là 16, đồng nghĩa với việc có 16 proton trong hạt nhân và 16 electron bao quanh nó.
Các đặc điểm cơ bản của nguyên tố lưu huỳnh (S)
| Tính chất | Giá trị |
|---|---|
| Tên nguyên tố | Lưu huỳnh (Sulfur) |
| Ký hiệu | S |
| Số hiệu nguyên tử | 16 |
| Nhóm trong bảng tuần hoàn | VIA (nhóm Chalcogen/Oxi) |
| Chu kỳ | 3 |
| Phân loại | Phi kim |
| Trạng thái tự nhiên | Rắn, màu vàng |
| Cấu hình electron | 1s² 2s² 2p⁶ 3s² 3p⁴ |
| Số oxi hóa thường gặp | -2, +4, +6 |
“Trong hóa học, lưu huỳnh luôn là một ví dụ kinh điển để minh họa cho khả năng biến hóa số oxi hóa của phi kim – từ -2 trong H₂S đến +6 trong H₂SO₄”, TS. Trần Quốc Hưng – Giảng viên Hóa học Phân tích.
Lưu huỳnh có ở đâu trong tự nhiên?
Lưu huỳnh là nguyên tố tương đối phổ biến trong vỏ Trái đất. Nó tồn tại ở cả ba dạng cơ bản:
- Dạng tự do: thường thấy dưới dạng các mỏ lưu huỳnh nguyên chất (chủ yếu ở núi lửa).
- Dạng kết hợp: xuất hiện trong khoáng vật như pyrite (FeS₂), galena (PbS) hoặc sphalerite (ZnS).
- Dạng hòa tan: dưới dạng ion sunfat (SO₄²⁻) trong nước biển, nước khoáng.
Bên cạnh đó, lưu huỳnh cũng rất quan trọng đối với sự sống vì:
- Là thành phần thiết yếu của axit amin (methionine, cysteine).
- Có mặt trong các enzyme sinh học quan trọng.
- Là vi chất cần thiết cho cây trồng – tương tự như bạn có thể thấy trong nội dung so sánh nguyên tố đa lượng và vi lượng.
Tính chất hóa học đặc trưng của lưu huỳnh
Như đã đề cập ở trên, lưu huỳnh có khả năng thể hiện nhiều số oxi hóa khác nhau, do đó cũng tham gia được nhiều phản ứng vô cơ quan trọng.
1. Phản ứng với kim loại
Lưu huỳnh dễ dàng kết hợp với kim loại ở nhiệt độ cao, cho ra muối sunfua:
Fe + S → FeS (muối sắt (II) sunfua, màu đen)Phản ứng này tỏa nhiệt mạnh và là thí nghiệm nổi tiếng trong chương trình phổ thông.
2. Phản ứng với phi kim
Khi phản ứng với oxi, lưu huỳnh tạo thành SO₂ – một khí không màu, mùi hắc:
S + O₂ → SO₂Khí này tiếp tục bị oxi hóa thành SO₃, chất quan trọng trong sản xuất axit sunfuric:
2SO₂ + O₂ ⇌ 2SO₃ (trong điều kiện có xúc tác)“SO₂ không chỉ là sản phẩm trung gian trong công nghiệp, mà còn là nguyên nhân gây mưa axit – một vấn đề môi trường nghiêm trọng”, PGS.TS Nguyễn Thị Mai Lan – Chuyên gia Công nghệ Hóa Môi Trường.
3. Phản ứng với dung dịch kiềm
Lưu huỳnh tác dụng với dung dịch kiềm như NaOH tạo ra hỗn hợp muối:
3S + 6NaOH → 2Na₂S + Na₂SO₃ + 3H₂OPhản ứng này thể hiện tính lưỡng tính oxi hóa – khử của lưu huỳnh.
Các hợp chất quan trọng của so (S)
Có vô số hợp chất mà lưu huỳnh tham gia tạo thành, nhưng nổi bật nhất bao gồm:
- Hidro sunfua (H₂S): khí mùi trứng thối, rất độc, xuất hiện trong khí sinh ra từ xác sinh vật phân hủy.
- Sắt(II) sunfua (FeS): tạo ra phản ứng đặc trưng với axit giải phóng khí H₂S.
- Lưu huỳnh đioxit (SO₂): nguyên liệu sản xuất axit sunfuric.
- Axít sunfuric (H₂SO₄): một trong những axit mạnh và quan trọng hàng đầu trong công nghiệp.
“H₂SO₄ như là xương sống cho toàn bộ ngành công nghiệp hóa chất – từ chế biến kim loại đến chế tạo phân bón, thuốc nhuộm”, Thầy Trần Quốc Hưng chia sẻ.
Lưu huỳnh – nguyên tố không thể thiếu trong đời sống
Dù đôi khi bị “lãng quên” sau oxi hay cacbon, lưu huỳnh đóng vai trò thiết yếu ở nhiều lĩnh vực:
Nông nghiệp
- Là vi chất thiết yếu cho cây trồng, giúp tổng hợp axit amin.
- Dạng phân bón chứa sunfat giúp cây phát triển khỏe mạnh.
Công nghiệp
- Sản xuất axit sunfuric – axit vô cơ quan trọng nhất thế giới.
- Tiền chất trong quá trình lưu hóa cao su, giúp tăng độ bền cho lốp xe, ủng nhựa, găng tay.
Y học và đời sống
- Thành phần trong thuốc kháng sinh nhóm sulfa.
- Dạng xà phòng hay kem lưu huỳnh dùng trị bệnh da liễu.
“Dù chỉ chiếm một phần rất nhỏ trong cấu tạo cơ thể, nhưng thiếu lưu huỳnh, cơ chế kháng viêm và trao đổi chất sẽ bị rối loạn nghiêm trọng”, BS. Nguyễn Thu Hiền – Chuyên khoa Dinh dưỡng Sinh học.
Hỏi – Đáp Nhanh: Những câu hỏi phổ biến về “so là nguyên tố gì”
Lưu huỳnh là kim loại hay phi kim?
=> Lưu huỳnh là phi kim. Nó không dẫn điện, dẫn nhiệt, và tồn tại ở dạng rắn màu vàng trong điều kiện thường.
Lưu huỳnh có độc không?
=> Ở dạng nguyên chất, lưu huỳnh không độc. Tuy nhiên, H₂S và SO₂ – các hợp chất chứa lưu huỳnh – có mùi hắc, độc và có hại nếu hít phải.
Lưu huỳnh có dẫn điện không?
=> Không. Lưu huỳnh tinh thể không dẫn điện và khó nóng chảy.
Vì sao gọi là so?
=> “So” là cách viết tắt hoặc đọc theo âm Hán – Việt của chữ “lưu huỳnh” trong ngôn ngữ hóa học.
Bổ sung kiến thức: Liên hệ với các nguyên tố phi kim khác
Nếu bạn đang tìm hiểu về các nguyên tố phi kim có tính chất tương đương hoặc thường kết hợp với so trong các phản ứng, đừng bỏ qua:
- Brom (Br) – Một halogen có tính oxi hóa mạnh, thường được so sánh với lưu huỳnh trong nhóm phi kim đặc trưng. Bạn có thể tìm hiểu thêm tại nguyên tố br.
- Na (Natri) – Kim loại kiềm dễ phản ứng, đóng vai trò quan trọng khi kết hợp với lưu huỳnh để tạo dạng muối như Na₂S. Chi tiết hơn tại nguyên tố na.
- Sg (Seaborgi) – Dù thuộc nhóm kim loại chuyển tiếp nặng, nhưng là nguyên tố kế tiếp trong bảng tuần hoàn sau lưu huỳnh về mặt chu kỳ. Tham khảo bài viết nguyên tố sg để mở rộng kiến thức.
Hình ảnh minh họa
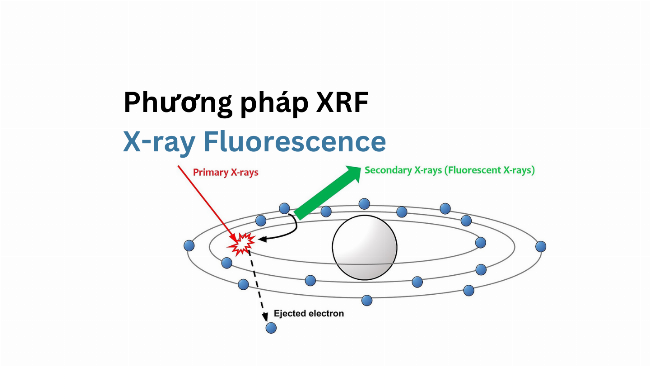 Cấu trúc nguyên tử nguyên tố lưu huỳnh với các lớp electron khác nhau
Cấu trúc nguyên tử nguyên tố lưu huỳnh với các lớp electron khác nhau
 Phản ứng hóa học của so với kim loại tạo muối sunfua
Phản ứng hóa học của so với kim loại tạo muối sunfua
Kết luận
Hy vọng rằng sau bài viết này, bạn đã có câu trả lời trọn vẹn cho thắc mắc “so là nguyên tố gì”. Lưu huỳnh không chỉ là một nguyên tố phổ biến về mặt hóa học, mà còn mang trên mình vai trò không thể thiếu trong đời sống, sức khỏe con người và sản xuất công nghiệp. Với khả năng biến hóa đa dạng về số oxi hóa và sự hiện diện toàn diện trong tự nhiên – lưu huỳnh xứng đáng là một trong những nguyên tố bạn cần ghi nhớ và tìm hiểu kỹ.
Bạn còn thắc mắc nào liên quan đến lưu huỳnh hay các nguyên tố hóa học khác? Hãy để lại bình luận hoặc lựa chọn bài viết phù hợp ngay trên “Hóa Học Phổ Thông” để tiếp tục hành trình khám phá thế giới nguyên tử thú vị!