Bạn có bao giờ tự hỏi tại sao nước biển lại có vị mặn không? Thật thú vị khi biết rằng điều này chủ yếu là nhờ vào muối Natri Clorua (NaCl), một hợp chất hóa học rất quen thuộc trong cuộc sống hàng ngày. Theo thống kê của Cục Hải Dương và Khí quyển Hoa Kỳ (NOAA), tỷ lệ muối NaCl trong nước biển chiếm khoảng 3,5%. Điều này có nghĩa là nếu có thể tách hết muối từ nước biển, chúng ta sẽ thu về tới 50 triệu tỷ tấn muối!
Nhưng NaCl – tính chất hóa học của nacl là muối gì và nó có những đặc điểm, ứng dụng ra sao? Hãy cùng hoahocphothong tìm hiểu một cách chi tiết và thú vị hơn về loại muối này nhé.
TÓM TẮT
Tính chất hóa học của NaCl? Định nghĩa và nguồn gốc
Tính chất hóa học của muối NaCl – Natri clorua (NaCl) là một hợp chất hóa học vô cơ với công thức NaCl.
Trong đó:
Na+ (natri) và Cl- (clorua) là hai ion liên kết với nhau.
Đây chính là thành phần chủ yếu trong muối ăn mà chúng ta sử dụng hàng ngày để làm gia vị hoặc chất bảo quản thực phẩm. Muối NaCl không chỉ tồn tại trong muối ăn mà còn có mặt trong nước biển, chất lỏng của các sinh vật sống, và thậm chí là thành phần quan trọng trong nhiều quá trình sinh hóa.
Về nguồn gốc, NaCl không chỉ có trong đại dương mà còn được tạo ra từ những hiện tượng tự nhiên khác. Phần lớn natri clorua trong nước biển có nguồn gốc từ quá trình bào mòn đá và khoáng chất trên mặt đất. Khi nước mưa rơi xuống, nó hòa tan khí CO2 từ không khí, trở nên có tính axit nhẹ. Khi dòng nước chảy qua các bề mặt đá, nó phá vỡ cấu trúc khoáng chất, tạo ra các ion như natri và clo. Những ion này sau đó được cuốn vào đại dương, nơi chúng kết hợp lại để tạo thành muối.
Không chỉ vậy, NaCl còn có nguồn gốc từ hoạt động của các núi lửa, nơi các hợp chất lưu huỳnh và các chất khoáng khác được giải phóng ra khỏi lòng đất. Sau khi núi lửa phun trào, các hợp chất này tiếp xúc với nước và không khí, tạo ra quá trình hình thành muối.
Cấu trúc tinh thể đặc biệt của NaCl
Natri clorua có cấu trúc tinh thể lập phương đơn giản, trong đó mỗi ion Cl– được bao quanh bởi 6 ion Na+, và ngược lại. Cấu trúc này tạo ra một mạng tinh thể bền vững, là đặc trưng của các hợp chất ion. Điều này cũng là lý do khiến NaCl có những tính chất vật lý đặc biệt như điểm nóng chảy và điểm sôi cao, cùng khả năng dẫn điện tốt ở trạng thái lỏng.
Cấu trúc tinh thể của NaCl còn được biết đến với tên gọi là cấu trúc halide, một kiểu cấu trúc phổ biến trong nhiều hợp chất khác như KCl (kali clorua) hay MgO (magie oxit). Các tinh thể NaCl thường có màu trắng hoặc không màu, tuy nhiên, trong một số điều kiện cụ thể, chúng có thể xuất hiện màu vàng nhẹ do sự hiện diện của các tạp chất.
Tính chất vật lý của NaCl
Muối NaCl là một chất rắn có kết tinh màu trắng hoặc không màu. Đây là một loại chất hút ẩm, có thể hấp thụ hơi nước từ môi trường xung quanh nếu độ ẩm tương đối vượt quá 75%. Một tính chất đáng chú ý khác của NaCl là nhiệt độ nóng chảy rất cao, đạt tới 801 độ C và bắt đầu bốc hơi ở nhiệt độ trên 1413 độ C.
NaCl hòa tan tốt trong nước và có độ tan 35.9 g/ml ở nhiệt độ 25 độ C. Điều thú vị là độ hòa tan này thay đổi khi có mặt các chất khác như NaOH hay HCl. Điều này có nghĩa là khi thêm các hợp chất này vào, khả năng hòa tan của NaCl sẽ giảm, tạo ra những ứng dụng đặc biệt trong công nghiệp.
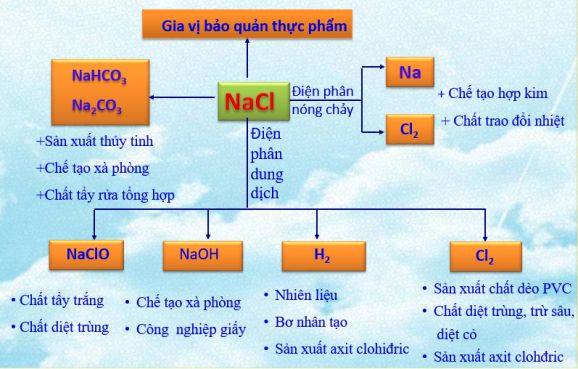
Tính chất hóa học của NaCl
Về tính chất hóa học, NaCl là một muối trung tính với pH = 7, không làm đổi màu quỳ tím và khá bền vững về mặt hóa học. Do là một hợp chất ion mạnh, NaCl dễ dàng phân ly hoàn toàn trong nước, tạo ra các ion Na+ và Cl-, làm cho dung dịch NaCl dẫn điện tốt. Tính chất điện li mạnh này là lý do NaCl được ứng dụng trong nhiều quá trình sản xuất công nghiệp.
NaCl cũng tham gia vào nhiều phản ứng hóa học quan trọng. Ví dụ, khi cho dung dịch NaCl phản ứng với AgNO3 (bạc nitrat), sẽ tạo ra AgCl (bạc clorua) kết tủa trắng, một phản ứng phổ biến trong các thí nghiệm phân tích hóa học.
Ngoài ra, NaCl còn phản ứng với axit sunfuric (H2SO4) để tạo ra khí HCl (axit clohidric) và NaHSO4. Đây là một phản ứng tiêu biểu được sử dụng trong quá trình sản xuất axit clohidric công nghiệp.
Sản xuất và khai thác muối NaCl
Sản xuất muối NaCl có ý nghĩa quan trọng trong nhiều lĩnh vực từ chế biến thực phẩm, y tế, đến công nghiệp. Trong tự nhiên, muối NaCl được sản xuất bằng cách cho nước biển bay hơi, thu được tinh thể muối. Những mỏ muối cũng là một nguồn cung cấp NaCl lớn. Các mỏ muối này hình thành từ hồ nước mặn hàng triệu năm trước, sau khi nước bốc hơi, để lại các vỉa muối khổng lồ dưới lòng đất.
Khám phá ngay chuyên mục “Tài liệu hóa học phổ thông” để nắm vững kiến thức từ cơ bản đến nâng cao!
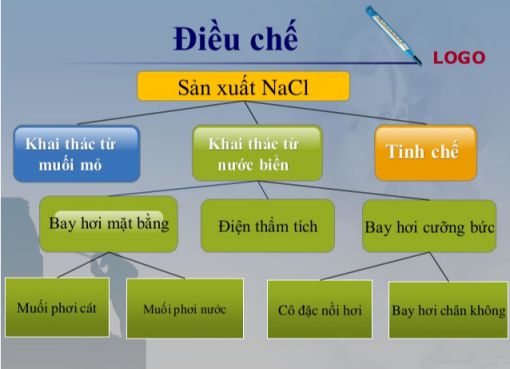
Tại các nước có biển, quá trình khai thác muối rất phổ biến. Người ta thường cho nước biển hoặc nước hồ mặn bay hơi dần trong các ô đựng nước, và sau một thời gian, muối sẽ kết tinh lại. Ở những nơi có mỏ muối, muối được khai thác bằng cách đào hầm sâu dưới lòng đất hoặc khoan giếng để đưa muối lên bề mặt.
Ứng dụng của muối NaCl trong đời sống
Muối NaCl không chỉ đơn giản là gia vị trong nấu ăn mà còn có rất nhiều ứng dụng quan trọng. Trong chế biến thực phẩm, muối được dùng để tăng hương vị, bảo quản thực phẩm khỏi bị hư hỏng. Trong lĩnh vực y tế, dung dịch muối sinh lý NaCl được sử dụng để điều trị mất nước, tiêu chảy và nhiều bệnh lý khác. Không chỉ vậy, trong công nghiệp, NaCl còn là nguyên liệu quan trọng để sản xuất xà phòng, chất tẩy rửa và nhiều hóa chất khác.
Kết luận
Qua bài viết này, chúng ta đã có cái nhìn toàn diện về NaCl, tính chất hóa học của nacl, định nghĩa, nguồn gốc, tính chất đến những ứng dụng trong cuộc sống. NaCl không chỉ là một loại muối quen thuộc mà còn là một hợp chất hóa học đóng vai trò không thể thiếu trong nhiều lĩnh vực khoa học và công nghiệp. Câu chuyện về nguồn gốc của muối NaCl cũng khiến chúng ta thêm hiểu về những quá trình tự nhiên kỳ diệu đã tạo nên sự phong phú và đa dạng của thế giới vật chất xung quanh.
Có thể bạn quan tâm: