Trong thế giới hóa học hữu cơ, hợp chất ankan giữ một vị trí nền tảng bởi sự đơn giản trong cấu trúc và tầm quan trọng trong nhiều phản ứng cũng như ứng dụng đời sống. Trong bài viết này, chúng ta sẽ cùng khám phá chi tiết về hợp chất ankan – từ định nghĩa, cấu tạo, tính chất hóa học cho đến ứng dụng thực tiễn – qua lăng kính dễ hiểu và gần gũi nhất với học sinh phổ thông.
Hợp chất ankan là nhóm hydrocarbon no đơn giản, đóng vai trò là “bài học vỡ lòng” cho bất kỳ ai bắt đầu tìm hiểu hóa học hữu cơ.
Ngay từ đầu bài viết, nếu bạn quan tâm đến phân loại chung của các loại hợp chất hữu cơ, đừng bỏ qua phần tổng quan tại bài viết hợp chất hữu cơ để nắm kiến thức nền vững chắc nhé.
TÓM TẮT
- 1 Hợp chất ankan là gì?
- 2 Cấu trúc phân tử của ankan
- 3 Danh pháp và đồng phân của ankan
- 4 Tính chất vật lý của hợp chất ankan
- 5 Tính chất hóa học đặc trưng của ankan
- 6 Sự khác biệt giữa ankan và các nhóm hydrocarbon khác
- 7 Ứng dụng và vai trò của hợp chất ankan
- 8 Các câu hỏi thường gặp về hợp chất ankan
- 9 Kết luận
Hợp chất ankan là gì?
Hợp chất ankan là một loại hydrocarbon no, trong đó các nguyên tử carbon liên kết với nhau bằng liên kết đơn và bão hòa hoàn toàn với nguyên tử hydro. Công thức tổng quát của chúng là CnH2n+2, trong đó n là số nguyên tử carbon.
Ví dụ về các ankan phổ biến:
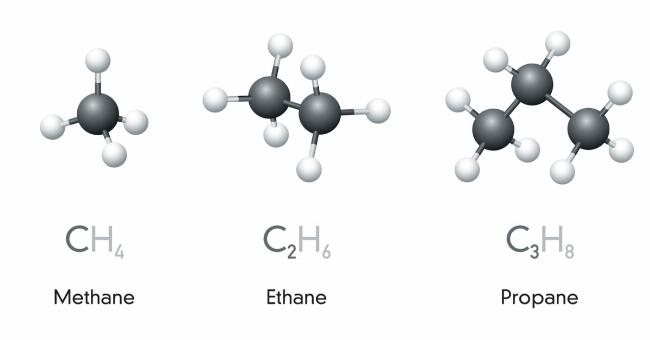
- Metan (CH₄)
- Etan (C₂H₆)
- Propan (C₃H₈)
- Butan (C₄H₁₀)
- Pentan (C₅H₁₂)
Đây là những cái tên quen thuộc, đặc biệt với metan và butan – những thành phần chính trong khí thiên nhiên và gas sử dụng hằng ngày.
“Ankan giống như những viên gạch đầu tiên xây dựng nên ngôi nhà hóa học hữu cơ.”
— Nguyễn Thị Mai Lan, giảng viên hóa học tại Trường THPT chuyên Khoa học Tự nhiên
Cấu trúc phân tử của ankan
Hợp chất ankan có cấu tạo mạch hở không phân nhánh hoặc phân nhánh, bao gồm các nguyên tử carbon liên kết với nhau bằng liên kết sigma (σ). Góc liên kết giữa các nguyên tử trong ankan thường là khoảng 109,5°, đặc trưng cho lai hóa sp³.
 Cấu trúc phân tử ankan cơ bản với liên kết đơn bão hòa và góc liên kết khoảng 109,5 độ
Cấu trúc phân tử ankan cơ bản với liên kết đơn bão hòa và góc liên kết khoảng 109,5 độ
Ankan không có nhóm chức đặc biệt, làm cho chúng tương đối trơ về mặt hóa học – nhưng chính sự “đơn giản” này lại khiến chúng trở thành đối tượng nghiên cứu quan trọng trong nhiều thí nghiệm cơ bản.
Danh pháp và đồng phân của ankan
Danh pháp:
- Danh pháp thông thường: metan, etan, propan,…
- Danh pháp IUPAC: bắt đầu từ các tiền tố chỉ số nguyên tử C (meth-, eth-, prop-,…) kết hợp với hậu tố “-an”.
Ví dụ:
- CH₄: metan
- C₂H₆: etan
- C₃H₈: propan
Đồng phân:
Từ butan (C₄H₁₀) trở đi, bắt đầu xuất hiện đồng phân mạch carbon:
- Butan → 2 đồng phân (butan thẳng và isobutan)
- Pentan → 3 đồng phân
Đồng phân tăng rất nhanh về số lượng khi số nguyên tử carbon tăng cao, đặc biệt ở các hợp chất có từ 6 nguyên tử carbon trở lên.
Tính chất vật lý của hợp chất ankan
Ankan có một số đặc điểm vật lý tương đối dễ nhớ:
| Tên ankan | Trạng thái ở nhiệt độ thường | Tan trong nước | Khối lượng riêng | Mùi |
|---|---|---|---|---|
| Metan đến Butan | Khí | Không tan | Nhẹ hơn nước | Không mùi |
| Pentan trở lên | Lỏng hoặc rắn | Rất khó tan | Gần bằng hoặc nặng hơn nước | Dầu nhẹ |
Tính tan yếu trong nước làm ankan được xếp vào nhóm các chất kỵ nước (hydrophobic), nhưng lại tan tốt trong dung môi hữu cơ như ete, benzen.
 Bảng thể hiện tính chất vật lý của các ankan phổ biến từ metan đến pentan
Bảng thể hiện tính chất vật lý của các ankan phổ biến từ metan đến pentan
Tính chất hóa học đặc trưng của ankan
Ankan dù khá ổn định nhưng vẫn có khả năng tham gia một vài phản ứng hóa học đáng chú ý:
1. Phản ứng cháy
Phản ứng phổ biến nhất và ứng dụng thiết thực trong đời sống:
CnH2n+2 + (3n+1)/2 O2 → nCO2 + (n+1)H2O
Ankan là nguồn năng lượng chính trong đốt nhiên liệu (gas, dầu hỏa…).
“Trong lớp học, phản ứng cháy ankan là ví dụ điển hình để minh họa định luật bảo toàn khối lượng.”
— Trần Quốc Hưng, giáo viên hóa học THPT tại Hà Nội
2. Phản ứng thế
Trong điều kiện nhiệt độ cao hoặc có ánh sáng, ankan có thể phản ứng thế với halogen (thế hydro bằng gốc halogen):
CH₄ + Cl₂ → CH₃Cl + HCl
Phản ứng này thường được dạy kỹ trong phần Tính chất hóa học của Ankan, bạn nên tham khảo để hiểu rõ thêm về cơ chế phản ứng.
3. Phản ứng nhiệt phân
Khi ankan bị đun nóng ở nhiệt độ rất cao có thể xảy ra cracking (phân cắt):
C₆H₁₄ → C₄H₈ + C₂H₆
Sản phẩm thường bao gồm anken (hydrocarbon không no) nên đây là bước khởi đầu dẫn đến tìm hiểu về các hợp chất như Anken.
Sự khác biệt giữa ankan và các nhóm hydrocarbon khác
| Đặc điểm | Ankan | Anken | Hợp chất Nitro |
|---|---|---|---|
| Liên kết | Chỉ liên kết đơn (σ) | Có ít nhất một liên kết đôi π | Có nhóm NO₂ |
| Bão hòa | Bão hòa | Không bão hòa | Bão hòa hoặc không |
| Phản ứng chính | Thế, cháy | Cộng, cháy | Phản ứng với kiềm, khử |
Bạn có thể tham khảo thêm tại hợp chất nitro nếu muốn mở rộng kiến thức về các nhóm chức năng khác nhau trong hóa học hữu cơ.
Ứng dụng và vai trò của hợp chất ankan
Ankan hiện diện khắp nơi xung quanh chúng ta, từ bếp gas, xe máy, máy bay cho đến các sản phẩm nhựa, dung môi:
- Năng lượng: nhiên liệu trong bếp gas (butan, propan)
- Công nghiệp hóa dầu: nguyên liệu sản xuất anken qua cracking
- Dung môi hữu cơ: hexan, heptan dùng trong điều chế, chiết tách
- Chất làm sạch công nghiệp
 Các ứng dụng thực tế của hợp chất ankan trong công nghiệp, năng lượng và đời sống
Các ứng dụng thực tế của hợp chất ankan trong công nghiệp, năng lượng và đời sống
Các câu hỏi thường gặp về hợp chất ankan
Hợp chất ankan có phản ứng cộng không?
Không, vì ankan không chứa liên kết đôi hoặc ba nên không tham gia phản ứng cộng như anken hay ankin.
Có bao nhiêu đồng phân cấu tạo của C₆H₁₄?
Có 5 đồng phân khác nhau về mạch carbon.
Ankan có tan được trong nước không?
Không hoặc rất ít tan vì chúng là các phân tử không phân cực, còn nước là dung môi phân cực.
Làm sao phân biệt ankan và anken trong phòng thí nghiệm?
Dùng dung dịch brom: anken làm mất màu brom, còn ankan thì không — giống như thí nghiệm minh họa khi tìm hiểu Tính chất hóa học của Metan hoặc anken.
Kết luận
Hợp chất ankan tuy đơn giản về cấu trúc nhưng lại là bước khởi đầu quan trọng trong hóa học hữu cơ. Chúng cung cấp nền tảng vững chắc để hiểu các nhóm hydrocarbon khác phức tạp hơn, đồng thời đóng vai trò không thể thiếu trong ngành năng lượng và công nghiệp hóa dầu. Việc nắm rõ về hợp chất ankan sẽ giúp bạn tự tin hơn khi tiếp tục chinh phục môn hóa học.
Bạn đã hiểu rõ hợp chất ankan là gì chưa? Nếu còn thắc mắc, đừng ngần ngại để lại bình luận bên dưới hoặc khám phá thêm các bài viết chuyên sâu khác để tiếp tục hành trình khám phá thế giới hóa học phong phú này.