Axit sunfuric (H2SO4) là một chất hóa học đóng vai trò cực kỳ quan trọng trong đời sống và công nghiệp. Được ví như “vua” của các hóa chất, H2SO4 có mặt trong hầu hết các lĩnh vực, từ sản xuất phân bón, xử lý nước, đến các phản ứng hóa học trong phòng thí nghiệm. Tuy nhiên, để hiểu và sử dụng axit sunfuric một cách an toàn, cần nắm rõ các tính chất, ứng dụng và lưu ý cần thiết khi tiếp xúc với loại hóa chất này. Bài viết này hoahocphothong sẽ cung cấp một cái nhìn tổng quan và Tính chất hóa học của H2SO4 loãng kỹ càng cho bạn học cùng hiểu nhé.
TÓM TẮT
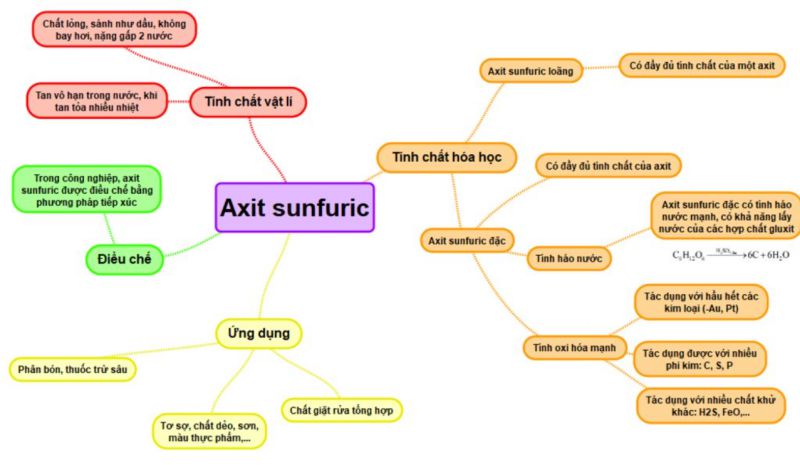
Tính chất hóa học của H2SO4 loãng là gì? (H2SO4)
Tính chất hóa học của H2SO4 loãng : Axit sunfuric là một trong những axit vô cơ mạnh nhất, có công thức hóa học là H2SO4. Đây là một chất lỏng không màu, không mùi và không bay hơi. Axit sunfuric nặng hơn nước và có khả năng hòa tan trong nước ở bất kỳ tỷ lệ nào, điều này làm cho nó trở thành một trong những dung dịch được ứng dụng rộng rãi trong nhiều ngành công nghiệp.
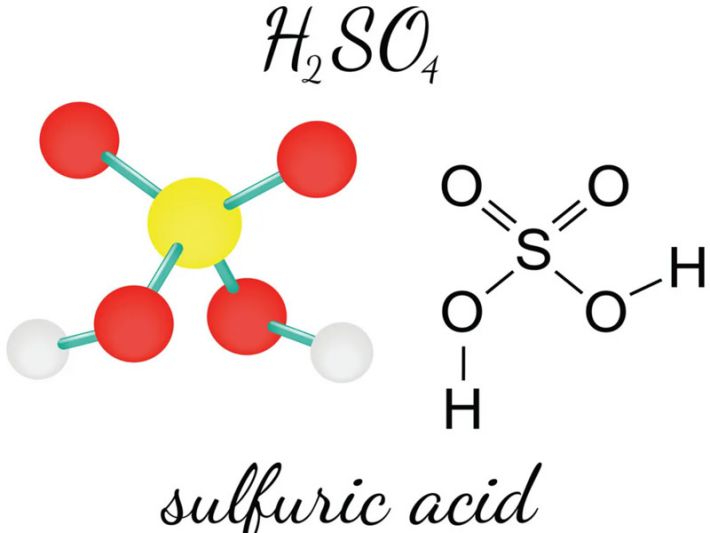
Axit sunfuric không tồn tại ở dạng tinh khiết trong tự nhiên mà chỉ có thể được sản xuất thông qua các quá trình phản ứng hóa học trong phòng thí nghiệm. Đặc biệt, một trong những ứng dụng phổ biến của H2SO4 mà chúng ta dễ dàng gặp phải là trong nước mưa. Khi axit sunfuric kết hợp với các thành phần khác trong khí quyển, nó có thể tạo ra mưa axit – một hiện tượng tự nhiên mà ai trong chúng ta cũng từng trải qua.
Tính chất hóa học của H2SO4 loãng & Tính chất vật lý
Tính chất hóa học của axit loãng này & tính chất vật lý: Axit sunfuric tồn tại dưới hai dạng chính: axit sunfuric loãng và axit sunfuric đặc, mỗi loại có những tính chất khác nhau.
Tính chất vật lý của H2SO4:
Axit sunfuric là một chất lỏng không màu, không mùi, và không vị.
Loại axit đặc có khả năng hút nước rất mạnh và tỏa ra nhiều nhiệt khi pha loãng. Điều này đòi hỏi phải tuân thủ nguyên tắc “cho axit vào nước”, không được làm ngược lại để tránh nguy cơ bị bỏng hóa chất.
Tính chất hóa học của H2SO4 loãng :
- H2SO4 loãng: Là một axit mạnh có đầy đủ các tính chất hóa học cơ bản của axit. Nó có khả năng làm đổi màu quỳ tím thành đỏ, phản ứng với kim loại, bazơ, oxit bazơ và muối để tạo ra nhiều hợp chất khác nhau.
- H2SO4 đặc: Không chỉ có các tính chất của axit loãng, axit sunfuric đặc còn có tính háo nước mạnh. Khi đổ H2SO4 đặc vào đường trắng, chẳng hạn, đường sẽ chuyển thành màu đen và tạo ra phản ứng phun trào.
Các Dạng Axit Sunfuric
Axit sunfuric tồn tại ở nhiều dạng tùy theo mục đích sử dụng:
Axit loãng (10%): Dùng trong các thí nghiệm hóa học cơ bản.
Axit dùng cho ắc quy (33,5%): Thường thấy trong các loại bình ắc quy.
Axit sản xuất phân bón (62,18%): Đây là tỷ lệ axit phổ biến trong sản xuất phân bón.
Axit Glover (77,67%): Sử dụng trong quá trình sản xuất axit glover.
Axit đậm đặc (98%): Dùng trong các phản ứng hóa học công nghiệp cần axit mạnh.
Khám phá ngay chuyên mục “Tài liệu hóa học phổ thông” để nắm vững kiến thức từ cơ bản đến nâng cao!
Ứng Dụng của H2SO4
Trong sản xuất công nghiệp: H2SO4 là thành phần không thể thiếu trong các ngành luyện kim, sản xuất chất tẩy rửa, sợi, giấy và phẩm nhuộm. Hằng năm, hơn 160 triệu tấn axit sunfuric được sản xuất để đáp ứng nhu cầu này.
Trong phòng thí nghiệm: Axit sunfuric được sử dụng để điều chế nhiều loại axit khác yếu hơn như HNO3, HCL, và trong các phản ứng hóa học khác.
Xử lý nước thải: H2SO4 có vai trò quan trọng trong việc xử lý nước thải. Nó được dùng để điều chế nhôm hydroxit, một thành phần quan trọng trong việc lọc tạp chất, khử mùi và cân bằng độ pH của nước, giúp loại bỏ các kim loại nặng gây ô nhiễm như Mg, Ca.
Sản xuất phân bón: Axit sunfuric là nguyên liệu chính trong sản xuất các loại phân bón như Phosphate, Canxi dihydrogen, Amoni Sunfat và nhiều loại khác.
Các ứng dụng khác: H2SO4 còn được sử dụng để sản xuất nhôm sunfat, một hợp chất quan trọng trong ngành sản xuất giấy. Nó phản ứng với xà phòng trong các sợi bột giấy để tạo ra các bề mặt cứng cho giấy.
Lưu Ý Khi Sử Dụng và Bảo Quản H2SO4
Khi sử dụng: Để đảm bảo an toàn, khi pha loãng axit sunfuric, luôn luôn cho từ từ axit vào nước và khuấy đều. Tuyệt đối không được làm ngược lại để tránh nguy cơ bỏng. Sử dụng găng tay, kính bảo hộ khi làm việc với axit loãng, và dùng mặt nạ, áo bảo hộ khi tiếp xúc với axit đậm đặc.
Bảo quản: H2SO4 là một chất hóa học rất mạnh và có tính ăn mòn cao. Vì vậy, cần bảo quản axit ở nơi khô ráo, tránh xa các chất bazơ và chất khử. Ngay cả khi đã pha loãng, axit sunfuric vẫn có khả năng ăn mòn kim loại như sắt và nhôm.
Như vậy,Tính chất hóa học của H2SO4 loãng – Axit sunfuric (H2SO4) là một hợp chất không thể thiếu trong nhiều lĩnh vực của cuộc sống, từ công nghiệp đến phòng thí nghiệm. Tuy nhiên, để sử dụng an toàn và hiệu quả, cần nắm rõ các tính chất và tuân thủ quy trình bảo quản, sử dụng đúng cách.
Có thể bạn quan tâm:
- Tính Chất Hóa Học Của H2SO4 Đặc Trong Thế Giới Hóa Chất
- Tìm Hiểu Tính Chất Hóa Học Của HCl
- Tinh Chất Hóa Học Của HNO3 Và Quy Trình Sản Xuất Axit Nitric