Bazơ là một trong những nhóm hóa chất quan trọng không chỉ trong lĩnh vực hóa học mà còn trong đời sống hàng ngày và sản xuất công nghiệp. Trong bài viết này, hãy cùng hoahocphothong tìm hiểu khái niệm về bazơ, các tính chất hóa học đặc trưng, và ứng dụng thực tế của nó. Hãy cùng khám phá ngay nhé!
TÓM TẮT
Bazơ Là Gì?
Bazơ được định nghĩa là hợp chất hóa học có phân tử bao gồm một nguyên tử kim loại liên kết với một hoặc nhiều nhóm hydroxit (OH). Hóa trị của kim loại trong bazơ tương đương với số lượng nhóm hydroxit. Định nghĩa khác là, tính chất hóa học của Bazo là các chất hòa tan trong nước và có độ pH lớn hơn 7 khi ở dạng dung dịch. Đây là điểm mấu chốt để phân biệt bazơ với các chất khác trong hóa học.
Tính chất hóa học của Bazo được phân loại chủ yếu dựa vào tính tan của chúng trong nước, dẫn đến hai loại chính:
1. Bazơ Tan Trong Nước (Kiềm)
Những bazơ này có khả năng hòa tan trong nước và tạo thành dung dịch bazơ, được gọi là kiềm. Một số ví dụ điển hình bao gồm:
Natri Hydroxit (NaOH)
Kali Hydroxit (KOH)
Bari Hydroxit (Ba(OH)₂)
Canxi Hydroxit (Ca(OH)₂)
Liti Hydroxit (LiOH)
Rubidi Hydroxit (RbOH)
Xesi Hydroxit (CsOH)
Stronti Hydroxit (Sr(OH)₂)
Cùng chủ đề:
2. Bazơ Không Tan Trong Nước
Ngược lại, một số bazơ không tan trong nước và không tạo thành dung dịch kiềm. Một số ví dụ về bazơ không tan trong nước bao gồm:
Đồng Hydroxit (Cu(OH)₂)
Magie Hydroxit (Mg(OH)₂)
Sắt (III) Hydroxit (Fe(OH)₃)
Alumin Hydroxit (Al(OH)₃)
Cùng chủ đề:
Công Thức Của Bazơ
Công thức chung của bazơ có thể được biểu diễn như sau:
M(OH)n\text{M(OH)}_nM(OH)n
Trong đó:
- M là bất kỳ kim loại nào,
- n là hóa trị của kim loại đó.
Tên gọi của bazơ được xác định theo trình tự: Tên bazơ = Tên kim loại (kèm theo hóa trị nếu cần) + hydroxit. Ví dụ:
- Natri hydroxit: NaOH
- Sắt (III) hydroxit: Fe(OH)₃
- Đồng hydroxit: Cu(OH)₂
Tính Chất Vật Lý Của Bazơ
Bazơ có một số tính chất vật lý đặc trưng như sau:
- Có độ nhờn giống như xà phòng.
- Có mùi và vị đắng đặc trưng.
- Bazơ ở nồng độ cao có khả năng ăn mòn mạnh mẽ với các chất hữu cơ và tác dụng mạnh với axit.
- Độ pH lớn hơn 7, cho thấy tính kiềm.
- Thường tồn tại dưới dạng rắn, bột hoặc dung dịch.
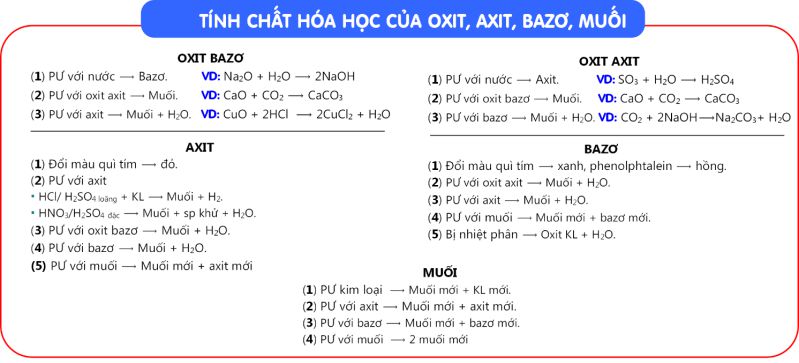
Tính Chất Hóa Học Của Bazo
Tính chất hóa học của Bazo quan trọng mà bạn cần biết:
- Thay Đổi Màu Chất Chỉ Thị:
- Bazơ có khả năng làm đổi màu quỳ tím thành xanh.
- Dung dịch phenolphthalein sẽ chuyển thành màu hồng khi gặp bazơ.
- Dung dịch methyl sẽ chuyển thành màu vàng.
- Phản Ứng Với Oxit Axit:
- Khi bazơ tác dụng với oxit axit, sản phẩm tạo ra là muối và nước. Ví dụ:
2NaOH + SO₂ → Na₂SO₃ + H₂O
- Khi bazơ tác dụng với oxit axit, sản phẩm tạo ra là muối và nước. Ví dụ:
- Phản Ứng Với Axit:
- Bazơ và axit phản ứng với nhau để tạo ra muối và nước. Ví dụ:
KOH + HCl → KCl + H₂O
- Bazơ và axit phản ứng với nhau để tạo ra muối và nước. Ví dụ:
- Phản Ứng Với Muối:
- Khi bazơ tác dụng với muối, sẽ tạo ra muối mới và bazơ mới. Ví dụ:
2KOH + CuSO₄ → K₂SO₄ + Cu(OH)₂↓
- Khi bazơ tác dụng với muối, sẽ tạo ra muối mới và bazơ mới. Ví dụ:
- Nhiệt Phân Hủy:
- Bazơ không tan có thể bị phân hủy khi chịu nhiệt, ví dụ:
Cu(OH)₂ → CuO + H₂O
- Bazơ không tan có thể bị phân hủy khi chịu nhiệt, ví dụ:
Khám phá ngay chuyên mục “Tài liệu hóa học phổ thông” để nắm vững kiến thức từ cơ bản đến nâng cao!
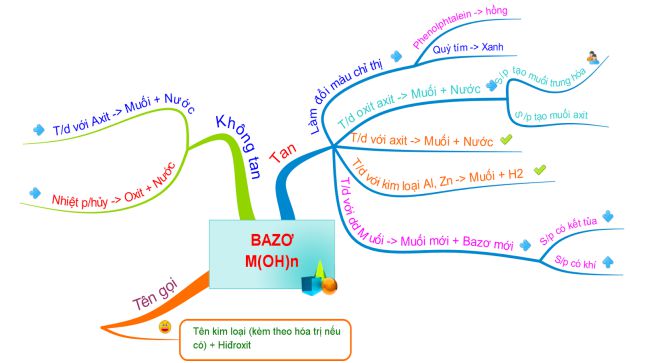
Cách Phân Loại Bazơ
Bazơ có thể được phân loại theo nhiều tiêu chí khác nhau:
- Theo tính chất hóa học của Bazo:
- Bazơ mạnh: NaOH, KOH…
- Bazơ yếu: Fe(OH)₃, Al(OH)₃…
- Theo Tính Hòa Tan Trong Nước:
- Bazơ tan trong nước: NaOH, KOH, Ca(OH)₂…
- Bazơ không tan trong nước: Cu(OH)₂, Mg(OH)₂…
Phương Pháp Điều Chế Bazơ
Trong phòng thí nghiệm, có thể điều chế bazơ qua một số phương pháp đơn giản:
Kim loại + nước → dung dịch bazơ + H₂
Oxit bazơ + nước → dung dịch bazơ
Điện phân dung dịch muối clorua hoặc bromua
Muối + bazơ → muối + bazơ
Ứng Dụng Của Bazơ
Bazơ có nhiều ứng dụng quan trọng trong thực tiễn:
Trong Phòng Thí Nghiệm: Dùng để học tập và nghiên cứu.
Trong Ngành Công Nghiệp Hóa Chất: Được sử dụng để sản xuất sản phẩm có nguồn gốc sodium như Javen, nước tẩy trắng và chất khử trùng.
Trong Ngành Công Nghiệp Dệt Nhuộm: Dùng để xử lý vải, giúp vải hấp thụ màu sắc tốt hơn.
Trong Nông Nghiệp: Được sử dụng như một chất khử trùng hiệu quả.
Trong Ngành Xây Dựng: Sử dụng trong sản xuất vôi, cải thiện độ chua của đất.
Một Số Bazơ Quan Trọng
Dưới đây là một số bazơ quan trọng mà bạn có thể thường xuyên gặp trong thực tế:
Natri Hydroxit (NaOH): Một bazơ mạnh, được sử dụng phổ biến trong sản xuất xà phòng, giấy, và trong các phòng thí nghiệm.
Canxi Hydroxit (Ca(OH)₂): Hay còn gọi là vôi tôi, được sử dụng trong xử lý nước và cải tạo đất.
Kết Luận
Bazơ là một phần thiết yếu của hóa học và có mặt trong nhiều khía cạnh của cuộc sống hàng ngày. Hy vọng rằng qua bài viết này, bạn đã có cái nhìn tổng quan và sâu sắc hơn về bazơ, các tính chất hóa học của nó, cũng như những ứng dụng trong thực tế. Đừng quên truy cập website hoachat.com.vn để tìm hiểu thêm nhiều thông tin bổ ích khác nhé!
Có thể bạn quan tâm:











